Lineární nerovnovážná termodynamika
V rovnovážném stavu jsou termodynamické síly a toky nulové, nulová je rovněž produkce entropie. Bude-li se systém od rovnovážného stavu vzdalovat, budou zobecněné termodynamické síly a toky spojitě narůstat. Omezíme-li se na studium systémů ve stavech dostatečně blízko rovnovážného stavu, je možné považovat závislost zobecněných termodynamických toků na silách za lineární.
Oblast termodynamických sil a toků, kde můžeme tuto aproximaci učinit, nazýváme lineární oblastí, termodynamiku vycházející
z uvedené aproximace nazýváme lineární nerovnovážnou termodynamikou. Oblast, kde lineární vztahy neplatí, nazýváme nelineární oblastí a studuje ji nelineární nebo zobecněná termodynamika.
1. Lineární fenomenologické zákony
V lineární oblasti vyjadřujeme závislost zobecněných toků na zobecněných termodynamických silách ve tvaru tzv. lineárních fenomenologických zákonů:
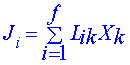 ,
, ![]() (1)
(1)
kde Lik jsou konstantní (nezávislé na Xk ) a nazýváme je fenomenologické koeficienty. Koeficienty typu Lii nazýváme vlastní a koeficienty typu Lik (i je různé od k) vzájemné (interferenční). Lineární fenomenologické zákony nejsou výsledkem samotné teorie, nýbrž jsou důsledkem experimentálních zkušeností a do teorie byly zavedeny ad hoc. Obsahují experimentální zkušenost, že jedna termodynamická síla může být příčinou několika toků a jeden tok může být vyvolán několika termodynamickými silami.
Koeficienty Lik mohou být v rámci fenomenologické teorie určeny buď experimentálně, nebo pomocí vhodně zvoleného kinetického modelu. Přesto je však velkým přínosem nerovnovážné termodynamiky v lineární oblasti to, že dovoluje stanovit a předvídat některé vlastnosti fenomenologických koeficientů Lik v obecném kontextu, tj. nezávisle na konkrétních fyzikálních podmínkách či zvoleném kinetickém modelu.
Po dosazení lineárních vztahů do vztahu pro produkci entropie dostaneme vztah pro hustotu produkce entropie v lineární oblasti
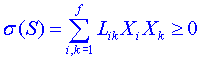 . (2)
. (2)
Rovnítko nastane právě ve stavu rovnováhy. Je též vidět, že v důsledku druhého termodynamického zákona je![]() v lineární oblasti pozitivně semidefinitní kvadratická forma proměnných Xi. Z toho vyplývá, že koeficienty nebudou naprosto libovolné, neboť kvadratická forma v proměnných Xi je pozitivně definitní, pokud jsou splněny tzv. Sylvestrovy podmínky. Tyto podmínky pro koeficienty Lik kvadratické formy lze vyjádřit pomocí odpovídajících matic koeficientů Lik a mají tvar
v lineární oblasti pozitivně semidefinitní kvadratická forma proměnných Xi. Z toho vyplývá, že koeficienty nebudou naprosto libovolné, neboť kvadratická forma v proměnných Xi je pozitivně definitní, pokud jsou splněny tzv. Sylvestrovy podmínky. Tyto podmínky pro koeficienty Lik kvadratické formy lze vyjádřit pomocí odpovídajících matic koeficientů Lik a mají tvar
![]()
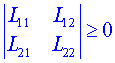
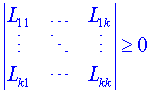 .
.
Vytvářejí tedy pro koeficienty Lik určitá omezení. Jak se ukazuje, jsou podmínky ve shodě s experimentálními výsledky, což je možno považovat za další důkaz platnosti druhého termodynamického zákona. Je totiž známo, že vlastní fenomenologické koeficienty Lii, jako např. koeficient tepelné vodivosti Lii, koeficient difúze LDD nebo elektrické vodivosti Lee jsou vždy kladné, naproti tomu co koeficient termodifúze LqD může být kladný i záporný.
Příklady lineárních fenomenologických zákonů
- Fourierův zákon pro přenos tepla vedením v lineární oblasti v důsledku gradientu teploty ![]() ,
,
![]() ,
,
kde jq je hustota tepelného toku a Lqq je koeficient tepelné vodivosti
- Fickův zákon difúze
![]() ,
,
(jD je hustota difúzního toku a LDD je difúzní koeficient) pro transport látky v důsledku gradientu koncentrace ![]() .
.
- Ohmův zákon elektrické vodivosti
![]() ,
,
(Lee je elektrická vodivost) o úměrnosti hustoty elektrického proudu je gradientu elektrického potenciálu ![]() .
.
- Newtonův zákon vazkosti
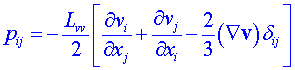
je vztah disipativní části tenzoru tlaku pij a gradientu rychlostního pole ![]() , kde
, kde ![]() je koeficient vazkosti uvažované tekutiny.
je koeficient vazkosti uvažované tekutiny.
2. Curieův-Prigoginův princip
Lineární fenomenologické zákony určují vztah mezi zobecněným tokem Ji a všemi zobecněnými silami Xi, které v systému působí. Tento vztah je vyjádřen prostřednictvím fenomenologických koeficientů Lik. Pro termodynamický systém mohou být zobecněné síly Xi (a odpovídající toky Ji) veličiny skalární (chemické reakce), vektorové (vedení tepla, difúze) i tenzorové (viskózní jevy). Ze vztahů pak plyne, že i koeficienty Lik mohou mít obecně tenzorový charakter. Skalár je tenzorem nultého řádu a vektor tenzorem prvního řádu. Vzniká otázka, zda se mohou vzájemně ovlivňovat procesy
s rozdílným tenzorovým charakterem.
P. Curie upozornil první na to, že ve statických systémech může vztah mezi příčinou a následkem, který způsobila, záviset
na prostorové symetrii těchto systémů. I. Prigogine zobecnil Curieho princip na termodynamické systémy: V izotropním termodynamickém systému (tj. systému, jehož vlastnosti jsou v rovnovážném stavu stejné ve všech směrech) v lineární oblasti, kde platí lineární fenomenologické zákony, se mohou vzájemně ovlivňovat (vázat) jenom nevratné procesy stejného tenzorového
charakteru. Tento poznatek pak nazýváme Curieovým-Prigoginovým principem.
Curieův-Prigoginův princip neplatí obecně v anizotropním prostředí a též pro stavy systému v nelineární oblasti. V těchto případech mohou právě v důsledku prostorové asymetrie a nelinearity procesů vzájemně interagovat i procesy s rozdílným tenzorovým charakterem.
To tedy znamená, že v lineárním izotropním systému nemůže afinita chemické reakce (skalární veličina) ovlivňovat difúzi nebo tepelnou vodivost (vektorové veličiny) a naopak. Na druhé straně však změna skalárního tlaku (ne hydrostatického tlaku p, který odpovídá elastickým změnám v prostředí) může být chemickou reakcí ovlivněna (a naopak).
Za výše uvedených podmínek Curieův-Prigoginův princip působí selektivně vzhledem ke smíšeným procesům a umožňuje předem vyloučit některé efekty, které bychom mohli obecně očekávat při interferenci různých nevratných procesů. Tím tento princip zjednodušuje i experimentální zkoumání smíšených procesů.
3. Onsagerovy relace reciprocity
Fenomenologické koeficienty Lik lze chápat jako vyjádření míry velikosti příspěvku jednotlivých nevratných procesů k zobecněnému toku, a tedy i k produkci entropie. Nabízí se otázka vztahu fenomenologických koeficientů, kterými stejné procesy přispívají k různým tokům.
Onsager ukázal, že v lineární oblasti je možno vždy zvolit zobecněné síly Xi a zobecněné toky Ji, charakterizující příslušné nevratné procesy, takovým způsobem, že je splněna podmínka (2) a zároveň pro všechny fenomenologické koeficienty platí
![]() (3)
(3)
Vztah nazýváme Onsangerovy relace reciprocity.Vyjadřují tu skutečnost, že když k toku Ji i-tého nevratného procesu přispívá síla Xk k-tého nevratného procesu měrou vyjádřenou fenomenologickým koeficientem Lik , pak též k toku Jk přispívá síla Xi stejnou měrou, vyjádřenou tímtéž fenomenologickým koeficientem Lik.
Onsagerovy relace reciprocity mají v lineární oblasti velký praktický význam. Umožňují totiž snížit počet fenomenologických koeficientů Lik téměř na polovinu, a tím zároveň snížit počet nezávislých experimentálních metod potřebných k jejich stanovení ve stejném poměru.
Vztahy (3) byly mnohokrát experimentálně ověřeny. Symetrie fenomenologických koeficientů není důsledkem druhého termodynamického zákona a nelze jí také dokázat pouze na základě postulátů a zákonů fenomenologické termodynamiky. V tomto smyslu můžeme tvrzení považovat za nový postulát pro lineární fenomenologickou termodynamiku. Jak ukázal Onsager, platnost (3) je možné dokázat na základě zákona mikroskopické vratnosti, podle kterého zákony pro mikroskopické objekty (jednotlivé částice) zůstávají nezměněny při inverzi času, tj. při transformaci t v - t.
V termodynamickém systému dochází neustále ke spontánním fluktuacím rozdělení energie i částic, dokonce i ve stavu rovnováhy. Pravděpodobnost vzniku určité fluktuace za určitou dobu po fluktuaci předešlé je stejná jako pro vznik stejných fluktuací v obráceném pořadí. V nelineární oblasti ztrácejí Onsagerovy relace reciprocity svou platnost. Koeficienty Lik mohou v této oblasti záviset
na zobecněných silách Xi a též vztahy mezi zobecněnými toky a silami jsou nelineární.
4. Princip minimální produkce entropie
Jednou z důležitých vlastností otevřených systémů je vytváření nerovnovážných stacionárních stavů. Uvažujme otevřený termodynamický systém
v lineární oblasti, který je popsán zobecněnými toky J1,. . ., Jf a zobecněnými silami X1, . . . , Xf . Pak v systému platí lineární fenomenologické zákony a Onsagerovy relace reciprocity. Předpokládejme, že v našem systému jsou síly X1, . . . , Xk udržovány
při konstantních hodnotách a síly Xk+1 , . . . , Xf se mohou libovolně měnit v čase. Ve stacionárním stavu musí být časová derivace produkce entropie rovna nule. Tuto derivaci můžeme vzhledem ke vztahu (2) vyjádřit ve tvaru
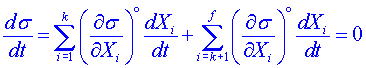 (4)
(4)
kde indexem ° označujeme, že derivace se berou ve stacionárním stavu. První člen na pravé straně rovnice (4) vymizí v důsledku nezávislosti termodynamických sil X1,…, Xk na čase. Avšak podle (2) můžeme veličiny 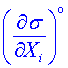 vyjádřit ve tvaru
vyjádřit ve tvaru
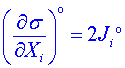 pro
pro ![]() . (5)
. (5)
Po dosazení do (4) dostaneme ekvivalentní podmínku stacionárnosti:
![]() . (6)
. (6)
Tato podmínka je ve shodě se známými experimentálními výsledky, podle nichž ve stacionárním stavu toky sdružené s proměnlivými zobecněnými silami vymizí. Podmínky stacionarity (6) jsou však podle (5) ekvivalentní podmínkám:
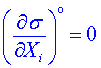 pro
pro ![]() , (7)
, (7)
což znamená, že ve stacionárním stavu je produkce entropie extrémní. Druh extrému zjistíme určením znaménka druhých derivací
ve stacionárním stavu. Podle (2) platí
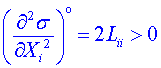 , (8)
, (8)
a tedy ve stacionárním stavu je v lineární oblasti produkce entropie minimální. Toto tvrzení je vyjádřením Prigoginova principu minimální produkce entropie: "Produkce entropie nabývá minimální hodnoty v tom stacionárním stavu, který je v souladu se zadanými hraničními podmínkami určenými charakterem úlohy." Prigoginův princip minimální produkce entropie nám umožňuje charakterizovat chování systému v blízkosti stacionárního stavu v lineární oblasti. Systém se bude vyvíjet do stacionárního stavu tak, že produkce entropie v čase bude klesat (tedy změna produkce entropie bude v čase záporná), až dosáhne minima právě ve stacionárním stavu. Evoluci systému do stacionárního stavu můžeme tedy popsat podmínkou
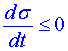 , (9)
, (9)
kdy rovnost nastane právě ve stacionárním stavu. Podmínce (9) se někdy též říká vývojové kritérium pro nevratné procesy v lineární oblasti. Produkce entropie představuje tak v lineární oblasti skalární potenciál, charakterizující vývoj systému.
Zpracováno podle:
Duršpek J. : Moderní termodynamika v chemických a biologických procesech, Plzeň, 2005
Dvořák I., Maršík I.: Biotermodynamika, Academia Praha 1998.
Maršík F.: Termodynamika kontinua, Academia, Praha 1999.
Prokšová J.: Entropie na středoškolské úrovni, MFF UK, Praha 2004.
Prigogine I., Kondepudi D.: Modern Thermodynamics, John Wiley & Sons, Chichester 1998.
Prigogine I.: Thermodynamic of Irreversible Processes, John Wiley and Sons, New York 1961.
Prigogine I., Stengers I.: Řád z chaosu, Mladá fronta, Praha 2001.
Tockstein A., Treindl L.: Chemické oscilace, Academia, Praha 1986.